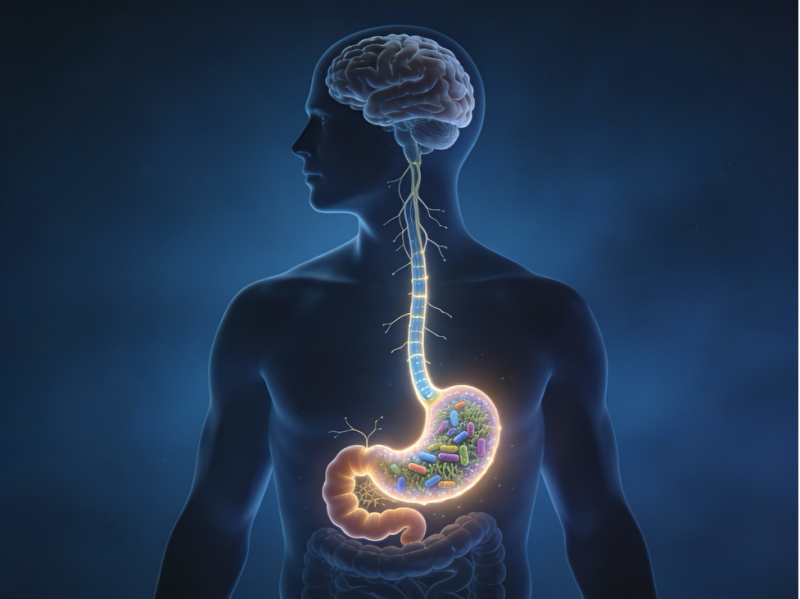
КИШЕЧНЫЙ МИКРОБИОМ И ОСЬ «КИШЕЧНИК—ГОЛОВНОЙ МОЗГ» В КЛИНИЧЕСКОЙ НУТРИЦИОЛОГИИ
АЛМАЗ ШАРМАН, профессор медицины
Введение: зачем специалисту по питанию «внутренний тропический лес»
Пищеварительная система — не просто трубка для переваривания пищи. Это сложная биологическая территория, где одновременно работают ферменты, гормоны, иммунные клетки и нервные структуры. Но есть ещё один участник, долго остававшийся «за кадром» классической медицины: кишечный микробиом — сообщество микроорганизмов, которые постоянно живут внутри нас.
Сегодня становится всё очевиднее: микробиом нельзя рассматривать как второстепенный фон. Он работает как функциональная система, способная влиять на метаболизм, барьер кишечника, иммунитет и даже нейропсихологическое состояние человека. И именно поэтому микробиом всё чаще обсуждают вместе с другой ключевой темой современной нутрициологии — осью «кишечник—головной мозг», где роль главного проводника связи играет блуждающий нерв.
Микробиом как экосистема: не список бактерий, а живая система
Толстая кишка является основным биотопом кишечного микробиома — совокупности микроорганизмов, обитающих в просвете кишечника и на поверхности слизистой. По численности речь идёт о триллионах клеток, среди которых доминируют бактерии, но также присутствуют вирусы, грибы и простейшие.
Важнее всего то, как на микробиом следует смотреть: это не перечень видов, которые можно разделить на «хороших» и «плохих». Микробиом — это многоуровневая экосистема, в которой микроорганизмы конкурируют за субстраты, вступают в кооперативные связи и формируют устойчивые функциональные контуры.
В клинической практике и образовательном контексте микробиом удобно понимать через два взаимосвязанных показателя:
- состав (соотношение таксонов и функциональных групп),
- разнообразие (видовое богатство и равномерность распределения).
Именно эти параметры оказываются значимыми для состояния кишечного барьера, иммунной регуляции и метаболического статуса.
Как мы изучаем микробиом: от невидимого мира к измеримому профилю
Долгое время значительная часть кишечных бактерий оставалась недоступной для исследования: многие из них анаэробны и не культивируются в стандартных лабораторных условиях. Ситуация изменилась, когда в практику вошли методы секвенирования ДНК, позволяющие оценивать микробный профиль по биологическим образцам (прежде всего по калу) и сопоставлять фрагменты генетического материала с референсными базами данных.
Это стало важным научным шагом: микробиом перестал быть абстрактным понятием и превратился в объект, который можно описывать, сравнивать и анализировать — пусть и с пониманием ограничений интерпретации.
Ключевые группы микробиома: «кто живёт в системе и что делает»
Когда специалист открывает отчёт по микробному профилю, он видит не одну «главную бактерию», а пропорции больших групп, каждая из которых связана с определёнными функциями.
Firmicutes (фирмикуты): эффективность извлечения энергии и риск метаболического смещения
Представители Firmicutes участвуют в ферментации пищевых компонентов и связаны с процессами извлечения энергии из рациона, включая метаболизм липидов. В исследованиях неоднократно отмечалось: повышение доли Firmicutes чаще встречается при рационе, богатом жиром и сахаром, и ассоциируется с риском избыточной массы тела.
При этом важно сохранять профессиональную осторожность: наблюдаемые связи не всегда означают прямую причинность — микробиом связан с образом питания и поведением, а не существует отдельно от них.
Bacteroidetes (бактероидеты): клетчатка, метаболиты и иммунное «обучение»
Группа Bacteroidetes функционально значима в контексте расщепления неперевариваемых пищевых волокон и образования метаболитов, поддерживающих физиологическое состояние кишечной стенки. Одновременно обсуждается их вклад в процессы «обучения» иммунной системы и регуляции воспалительных реакций слизистой.
Метаболиты микробиома: что происходит с пищей, которую человек не может переварить
Один из наиболее клинически важных принципов микробиологии питания звучит так: часть пищи не заканчивается в человеке — она продолжается в микробиоме.
Микробиом синтезирует метаболиты из субстратов, которые не расщепляются ферментами человека. Центральным продуктом этой ферментации являются короткоцепочечные жирные кислоты, среди которых особое значение имеет бутират (масляная кислота).
Бутират выполняет несколько функций, объединённых одной логикой: он помогает кишечнику сохранять структурную устойчивость и физиологическое равновесие. Он:
- поддерживает нормальную пролиферацию и дифференцировку клеток эпителия кишечника;
- способствует противовоспалительному профилю слизистой;
- поддерживает целостность барьера, уменьшая вероятность транслокации бактерий и токсинов.
С практической точки зрения это означает, что пищевые волокна — это не второстепенный компонент рациона, а субстрат для формирования биологически активных соединений, влияющих на воспаление и барьер.
Akkermansia: пример функционального «специалиста» кишечной экосистемы
Среди отдельных родов бактерий, привлекающих внимание исследователей, выделяют Akkermansia. Её уникальность состоит в способности использовать слизистый слой кишечника как источник питания, что связывают с потенциальной ролью в поддержании барьерной функции и снижении воспалительной активности.
Экспериментальные работы на животных показывали улучшение метаболических показателей при повышении доли Akkermansia. Однако исследования на людях продолжаются, и выводы требуют аккуратного переноса в клинические рекомендации.
Среди факторов, ассоциируемых с поддержанием этой группы, обсуждаются пищевые источники полифенолов и более структурированный режим питания, включая уменьшение постоянных перекусов. При этом важно подчеркнуть: речь идёт не о «магической бактерии», а о маркере и участнике комплекса условий, поддерживающих барьер и метаболическую устойчивость.
Кишечный барьер: где заканчивается пищеварение и начинается системная регуляция
Если микробиом — это экосистема, то слизистая оболочка кишечника — её граница. Она выполняет роль селективного барьера: пропускает питательные вещества и ограничивает проникновение микробов и их компонентов.
Когда межклеточные контакты ослабевают, формируется состояние, известное как повышенная кишечная проницаемость. В популярной литературе это часто называют «синдромом дырявого кишечника», но в академическом изложении предпочтительны термины, связанные с измеряемыми параметрами.
Клинически это состояние может сопровождаться вздутием, болевым синдромом, нарушениями стула, утомляемостью и пищевой чувствительностью. К факторам риска относят перенесённые инфекции, антибиотикотерапию, особенности диеты и выраженные стрессовые нагрузки.
Один из подходов к оценке проницаемости — тесты с растворами сахаров различной молекулярной массы и последующим измерением их соотношений в моче. Логика проста: малые молекулы проходят легче, крупные — хуже; при нарушении барьера меняется их соотношение.
Когда экосистема нарушается: патогены, антибиотики и «окно возможностей» для болезни
В кишечнике всегда присутствует потенциальное напряжение: наряду с симбиотическими и нейтральными микроорганизмами могут встречаться и те, кто способен вызывать заболевание при благоприятных условиях.
Пищевые инфекции: типичный сценарий «резкого вмешательства»
К частым причинам пищевых инфекций относят Campylobacter, патогенные штаммы E. coli и Salmonella. Профилактика здесь остаётся классической и клинически важной: термическая обработка продуктов животного происхождения, предотвращение перекрёстного загрязнения и соблюдение гигиены приготовления пищи.
Clostridioides difficile: патоген, который получает власть после антибиотиков
Особое место занимает Clostridioides difficile. Эта бактерия может присутствовать в кишечнике бессимптомно, но становится доминирующей после разрушения нормального микробного сообщества антибиотиками широкого спектра. Когда конкурентное давление снижается, C. difficile способна вызывать тяжёлую затяжную диарею.
Восстановление микробиома как терапия: логика трансплантации микробиоты
Трансплантация микробиоты применяется прежде всего при тяжёлых, рецидивирующих формах C. difficile-инфекции. В основе подхода лежит идея восстановить конкурентную среду и функциональные контуры микробиома, способные подавлять патоген.
При этом принципиально важно: безопасность процедуры определяется строгим скринингом доноров и стандартизацией протоколов; любые самостоятельные попытки переноса микробиоты недопустимы.
Разнообразие микробиома: критерий устойчивости и скорости восстановления
Чем разнообразнее микробное сообщество, тем устойчивее система к внешним воздействиям и тем быстрее она восстанавливается после эпизодов диареи или инфекционных факторов.
Снижение разнообразия связывают с тремя типичными обстоятельствами:
- пищевое однообразие и низкое потребление растительных волокон;
- высокая доля ультрапереработанных продуктов в рационе;
- частое или неоправданное применение антибиотиков.
Отдельного внимания заслуживает влияние некоторых пищевых добавок (например, эмульгаторов). Однако этот вопрос требует внимательной оценки качества доказательств, поскольку данное направление исследований продолжает находиться в стадии развития.
Начало истории: как микробиом формируется с первых лет жизни
Для клинициста важно помнить: микробиом не появляется одномоментно во взрослом возрасте — он строится с ранних этапов жизни. Он интенсивно формируется в первые годы, и значимыми факторами считаются способ рождения и характер вскармливания.
При вагинальных родах первичная колонизация чаще происходит микробами матери. При кесаревом сечении профиль первичной экспозиции иной и больше связан с микробами окружающей среды и кожи.
Грудное молоко, помимо нутриентов, содержит компоненты, которые в меньшей степени предназначены для прямого питания ребёнка и в большей — для поддержки роста определённых полезных бактерий. Это демонстрирует тесную биологическую связь между человеком и микробной экосистемой.
Микробиом, масса тела и обмен веществ: почему «калории» — не вся клиника
Энергетический баланс остаётся фундаментальным принципом, но в реальной практике он не объясняет всей сложности набора или снижения веса. Микробиом может влиять на массу тела по меньшей мере тремя путями:
- изменяя эффективность извлечения энергии из пищи;
- влияя на гликемический ответ и гормональные реакции;
- участвуя в регуляции аппетита через метаболиты и нейрогуморальные сигналы.
На этом фоне становится понятным: одинаковые продукты могут по-разному влиять на уровень глюкозы у разных людей, и одна из причин различий — совокупность факторов, включая состав микробиома.
Персонализированное питание: от универсальных рекомендаций к прогнозу реакции
Когда стали доступны инструменты непрерывного мониторирования глюкозы и параллельный анализ микробиома, выяснилось, что реакция на стандартные продукты существенно варьирует. На основе этих данных создаются модели, способные прогнозировать гликемический ответ и формировать персональные списки предпочтительных и нежелательных продуктов.
С научной точки зрения это направление перспективно, но требует долгосрочной валидации и оценки клинических исходов.
Ось «кишечник—мозг»: когда питание становится фактором поведения и эмоций
На определённом уровне нутрициология перестаёт быть исключительно про пищеварение. Кишечник обладает развитой нервной системой и связан с головным мозгом через блуждающий нерв и гуморальные пути.
Микробиом способен производить или модифицировать молекулы, влияющие на нейрохимические процессы, включая нейромедиаторные и гормональные сигналы. В экспериментальных моделях на животных доказательная база наиболее убедительна; у людей связь чаще носит ассоциативный характер, но клинические исследования с отдельными пробиотическими штаммами показывают возможность влияния на настроение и тревожность.
В профессиональном изложении корректно формулировать вывод осторожно: микробиом может смещать пищевые предпочтения и поведенческие реакции, но не заменяет влияние культуры, привычек, сна, стресса и доступности пищи.
Блуждающий нерв: главная магистраль связи тела и мозга
Мы живём в эпоху парадокса: медицина становится всё более технологичной, но всё больше людей ощущают, что организм словно «зависает» — не способен устойчиво перейти в режим восстановления. И здесь появляется герой, который не продаётся в аптеке и не существует в виде таблетки: блуждающий нерв.
Это один из самых длинных черепных нервов человека и одна из главных магистралей связи между мозгом и внутренними органами. По нему постоянно идёт поток сообщений: что происходит в кишечнике, насколько стабильно внутреннее состояние, есть ли воспаление, как работают сердце и дыхание.
Важная деталь анатомии: блуждающий нерв представлен двумя стволами — левым и правым. Каждый содержит около 100 тысяч волокон, вместе — порядка 200 тысяч аксонов. При этом примерно 80% волокон являются афферентными и передают информацию от органов к мозгу, что делает блуждающий нерв преимущественно сенсорной системой: мозг постоянно получает новости от тела.
Воспаление: от острой защиты к хроническому «воспалительному старению»
Острое воспаление легко узнаваемо: покраснение, жар, отёк, боль. Оно является защитной реакцией организма. Но один из ключевых вызовов современной медицины — хроническое воспаление, часто малозаметное, но устойчиво разрушающее регуляторные системы.
Это состояние называют inflammaging — «воспалительное старение», связанное с постоянным умеренным повышением провоспалительных медиаторов (TNF, IL-1, IL-6). Оно рассматривается как один из механизмов множества ведущих причин смертности: сердечно-сосудистых заболеваний, нейродегенерации, метаболических нарушений и онкологических процессов.
«Воспалительный рефлекс»: как нервная система регулирует иммунитет
Если воспаление так опасно в хроническом варианте, логично спросить: как организм его ограничивает? Один из ключевых ответов даёт холинергический противовоспалительный путь, связанный с блуждающим нервом.
Он может быть описан как рефлекторная дуга:
воспаление → мозг → блуждающий нерв → селезёнка → снижение цитокинов.
Этот механизм получил название «воспалительный рефлекс» и стал поворотной точкой в понимании того, что нервная система регулирует иммунные процессы так же, как регулирует дыхание или частоту сердечных сокращений.
Биоэлектронная медицина: лечение сигналом вместо вещества
Классическая фармакология действует через молекулярные мишени. Биоэлектронная медицина предлагает иную логику: воздействовать на нервные цепи, которые регулируют те же мишени «на месте», используя электрический сигнал.
Особенно важно, что стимуляция блуждающего нерва демонстрирует иной профиль безопасности по сравнению с полной блокадой цитокинов биологическими препаратами: она снижает патологически высокий уровень цитокинов примерно на 70%, возвращая его в физиологический диапазон и сохраняя иммунный ответ.
Микробиом → вагус → мозг: единая ось клинической регуляции
Связка «микробиом—воспаление—нервная система» перестаёт быть теоретической. В качестве примера приводят противосудорожный эффект кетогенной диеты, часть которого связывают с изменениями микробиоты, включая Akkermansia и Parabacteroides. Это иллюстрирует функциональную ось:
микробиом → вагус → мозг.
Стресс и питание: когда организм застревает в режиме «бей или беги»
Ось «кишечник—мозг» нельзя обсуждать без стрессовой эндокринологии. Хроническая активация стрессовой оси ведёт к избытку глюкокортикоидов, которые:
- усиливают глюконеогенез и липолиз,
- подавляют пищеварение, рост тканей и репродукцию,
- снижают чувствительность к инсулину,
- повышают риск гипергликемии.
В таком контексте блуждающий нерв становится механизмом переключения организма в режим восстановления — а значит, питание, сон и движение перестают быть «дополнением» и становятся базой регуляции.
Иммунная дисрегуляция и «гипотеза старых друзей»
Рост аллергических и аутоиммунных заболеваний долго объясняли «гигиенической гипотезой». Однако современная концепция делает акцент на другом: проблема не в том, что иммунитету «скучно», а в том, что он утратил контакт с микробами, которые исторически сопровождали человека и помогали иммунной системе обучаться различать «опасное» и «безопасное».
Сокращение контакта с такими микроорганизмами вследствие антибиотиков, пищевого однообразия и ультрапереработанных продуктов рассматривается как потенциальный фактор иммунной дисрегуляции.
Заключение: клиническое мышление о микробиоме как часть современной нутрициологии
Кишечный микробиом — это высокоорганизованная экосистема, влияющая на метаболизм, барьер, иммунную регуляцию и нейрогуморальные сигналы. И хотя часть факторов формирования микробиома задана ранними этапами жизни, значительная доля вариабельности у взрослых связана с модифицируемыми условиями.
В практическом смысле специалисту важно удерживать несколько ключевых идей:
- здоровье кишечника определяется составом и разнообразием микробиома;
- микробиом влияет на барьер через метаболиты, включая бутират, поддерживающий противовоспалительный баланс;
- антибиотики и пищевые инфекции могут разрушать устойчивость системы и создавать условия для доминирования патогенов;
- рацион, богатый растительными волокнами и разнообразием растений, остаётся базовой стратегией поддержки микробиома;
- ось «кишечник—головной мозг» через блуждающий нерв связывает питание с эмоциями, воспалением и метаболической устойчивостью, формируя новую клиническую перспективу работы с пациентом.