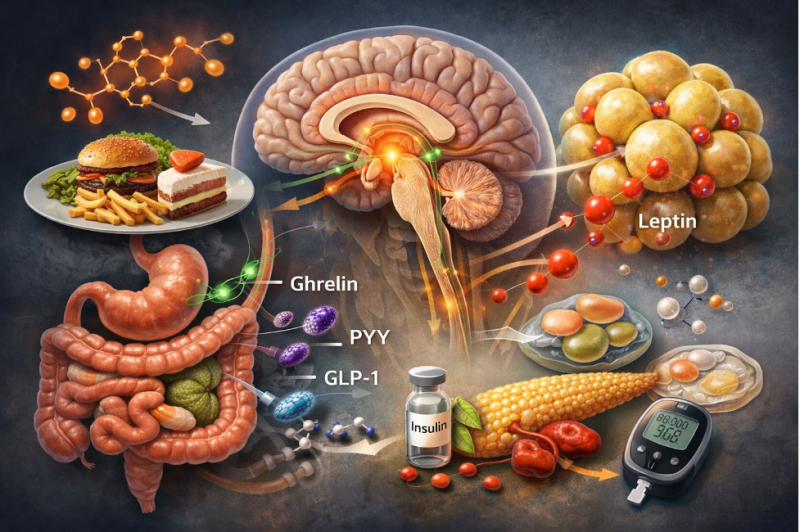
ГОРМОНАЛЬНАЯ РЕГУЛЯЦИЯ ПИТАНИЯ: ИНТЕГРАЦИЯ СИГНАЛОВ КИШЕЧНИКА, ЖИРОВОЙ ТКАНИ И ГОЛОВНОГО МОЗГА
АЛМАЗ ШАРМАН, профессор медицины
Введение: питание как физиологически управляемое поведение
Питание человека часто воспринимается как исключительно осознанный выбор: будто бы решение о том, что и сколько есть, всегда определяется знанием, дисциплиной и личной ответственностью. Однако современные данные физиологии, нейробиологии и эндокринологии показывают противоположное: пищевое поведение представляет собой биологически регулируемый феномен, формируемый интеграцией внутренних сигналов и факторов внешней среды.
Организм непрерывно сравнивает текущий метаболический статус с потребностями тканей и прогнозируемой доступностью энергии. Это сравнение реализуется через сложную систему сигналов — гормональных, нейрональных и гуморальных. Эти сигналы не «заставляют» человека есть механически, но существенно повышают или снижают вероятность пищевого поведения, направляя выбор продуктов, размеры порций, скорость приема пищи и субъективные ощущения голода и насыщения.
Центральная роль мозга в регуляции потребления пищи
Системная регуляция питания определяется работой центральной нервной системы, прежде всего гипоталамуса и связанных с ним нейрональных сетей. Именно мозг выступает интегратором сигналов, поступающих из жировой ткани, желудочно-кишечного тракта, поджелудочной железы и других органов.
Питание можно представить как цикл: периоды голода сменяются поиском еды, приемом пищи и насыщением. Важным является тот факт, что насыщение не всегда завершает потребление: возможны эпизоды еды при отсутствии физиологического голода, а также переедание, поддерживаемое эмоциональными и средовыми триггерами.
Таким образом, физиологическая регуляция питания включает как гомеостатическиемеханизмы (обеспечение энергетических и нутритивных нужд), так и гедонистические(пищевое удовольствие, мотивация, обучение и привычки), которые функционально переплетены и воздействуют друг на друга.
Гипоталамус: гомеостатический центр контроля энергии
Гипоталамус — ключевая структура мозга, обеспечивающая поддержание гомеостаза. Он участвует в контроле температуры, водного баланса, репродукции, дыхания и других жизненно важных процессов. В этом перечне важнейшее место занимает регуляция потребления пищи и энергетических запасов.
Классические нейрофизиологические наблюдения и эксперименты показали: повреждение определенных участков гипоталамуса может приводить либо к выраженной гиперфагии и набору массы тела, либо к резкому снижению аппетита вплоть до отказа от пищи. Это стало основой представления о мозговом контроле энергетического поведения.
Лептин: гормон жировой ткани как сигнал энергетических запасов
Лептин как «липостатический» сигнал
Одним из центральных достижений эндокринологии питания стало открытие лептина — гормона, вырабатываемого адипоцитами. Его концентрация в крови возрастает по мере увеличения запасов жировой ткани.
Лептин выполняет роль сигнала, информирующего мозг о количестве накопленной энергии. Его рецепторы представлены во многих тканях, но особенно концентрированы в гипоталамусе, где лептин участвует в регуляции аппетита и энергетических затрат.
Когда жировые запасы расходуются, уровень лептина снижается, и мозг воспринимает это как угрозу энергетическому балансу — что усиливает голод и поведенческую мотивацию к еде.
Лептин-дефицит и лептинорезистентность: клинические последствия
Классические генетические модели ожирения продемонстрировали два принципиально различных механизма:
- дефицит лептина как отсутствующий сигнал сытости на уровне организма;
- лептинорезистентность как нарушенное восприятие лептина мозгом при его высоком уровне.
Перенос этих данных в клиническую плоскость показал: хотя редкие формы ожирения обусловлены мутациями в лептиновой системе и могут драматически реагировать на заместительную терапию, подавляющее большинство пациентов с ожирением имеют высокий уровень функционального лептина, но слабый ответ на него. Это объясняет ограниченную эффективность лептин-терапии как универсального средства коррекции массы тела.
Временной масштаб действия лептина
Важно понимать, что лептин не является ведущим регулятором отдельного приема пищи. Он меняется относительно медленно и оказывает влияние преимущественно на горизонте недель и месяцев, корректируя деятельность нейрональных сетей, вовлеченных в краткосрочное пищевое поведение.
Кишечные гормоны: сигналы насыщения и голода
Желудочно-кишечный тракт как эндокринный орган
После открытия лептина было выявлено множество гормонов, которые продуцируются желудком и кишечником и участвуют в регуляции пищевого поведения. Важнейшая особенность — большинство таких гормонов отражают текущий процесс приема пищи, а значит имеют быстрое действие.
К числу наиболее значимых относятся:
- грелин,
- PYY,
- CCK,
- GLP-1.
Эти гормоны секретируются в кровь, а часть сигналов может передаваться локально через нервные волокна, связывающие кишечник с мозгом.
Грелин: гормон голода
Грелин является ключевым гормональным сигналом, усиливающим чувство голода. Его концентрация повышается перед приемом пищи и снижается после начала питания. Он действует как маркер «пустого желудка» и формирует предпосылку к поиску пищи.
PYY и CCK: вклад в развитие насыщения
PYY и CCK повышаются после приема пищи и рассматриваются как гормоны, способствующие формированию чувства насыщения. Они относятся к группе кишечных сигналов, которые помогают мозгу оценивать объем и питательную ценность поступившей еды.
Однако принципиально важно подчеркнуть: ни один кишечный гормон не действует как бинарный переключатель «есть/не есть». Эффект сигналов зависит от множества контекстов — состава пищи, сенсорной стимуляции, эмоционального состояния, обученных привычек и доступности еды.
GLP-1: эндокринная связь углеводного обмена и пищевого поведения
GLP-1 как инкретиновый и анорексигенный сигнал
GLP-1 первоначально приобрел клиническую значимость как гормон, усиливающий секрецию инсулина после приема пищи при повышении глюкозы в крови. Этот эффект критически важен для пациентов с сахарным диабетом 2 типа, поскольку позволяет улучшать постпрандиальную регуляцию гликемии.
Уникальность GLP-1 заключается в том, что он усиливает секрецию инсулина при высоком уровне глюкозы, но прекращает действие до развития гипогликемии, что повышает безопасность этого механизма.
GLP-1 и снижение массы тела: механизм через мозг
С увеличением фармакологического применения агонистов GLP-1 было замечено выраженное снижение массы тела, которое оказалось связано не только с периферическими метаболическими эффектами, но и с влиянием на центральную регуляцию потребления пищи.
Экспериментальные данные показывают: при выключении рецепторов GLP-1 в мозге препараты теряют эффект снижения массы тела, что подтверждает центральный механизм действия.
В то же время вопрос о том, каким образом циркулирующий GLP-1 влияет на мозг, сохраняется как активная научная проблема: предполагается участие структур с более проницаемым гематоэнцефалическим барьером, включая области заднего мозга, реагирующие на токсины и нутриенты крови.
Нейрональные механизмы голода: AgRP-нейроны как инициаторы пищевого поведения
В физиологии голода ключевое место занимает популяция нейронов гипоталамуса, известных как AgRP-нейроны. Их активация ассоциируется с запуском состояния голода и поискового поведения, направленного на получение пищи.
Экспериментальные данные показывают: стимуляция этих нейронов у сытых животных вызывает поведение, аналогичное выраженному голоду, и приводит к немедленному потреблению пищи. При начале питания их активность снижается под влиянием гормональных и нутриентных сигналов крови.
Особенно важным является уточнение современной нейробиологии: активность AgRP-нейронов может снижаться ещё до фактического поступления нутриентов — уже при виде и запахе пищи. Это отражает предиктивную природу регуляции: мозг может заранее снижать «аварийный» сигнал голода при ожидаемом поступлении энергии.
Дофамин и система вознаграждения: мотивация, обучение и пищевые привычки
Дофамин как медиатор мотивации
Хотя дофамин традиционно называют «гормоном удовольствия», более корректно рассматривать его как медиатор мотивации, побуждения и формирования направленного поведения. Он участвует в механизмах «подготовки к награде» и усиливает внимание к сигналам, предсказывающим получение значимого ресурса — в данном случае пищи.
При дефиците дофамина у животных развивается глубокая апатия: даже при доступности еды они могут не предпринимать действий для её получения, что демонстрирует критическую роль дофамина в мотивационном компоненте питания.
Условные сигналы и перенос дофаминовой реакции
Формирование пищевого поведения тесно связано с обучением. В классических моделях условного рефлекса дофаминовый всплеск постепенно смещается от самой еды к сигналу, который предсказывает её поступление. Таким образом, окружающая среда становится активным участником регуляции питания, поскольку визуальные и обонятельные стимулы способны запускать мотивационные реакции даже без физиологического голода.
Инсулин: регулятор гликемии и компонент аппетит-контроля
Инсулин рассматривается прежде всего как гормон углеводного обмена, однако он также вовлечен в регуляцию пищевого поведения. После приема пищи рост глюкозы стимулирует секрецию инсулина, что способствует утилизации глюкозы тканями и может участвовать в подавлении аппетита наряду с кишечными сигналами насыщения.
Это подчеркивает клиническую необходимость оценивать пищевое поведение не только через призму «калорий», но и через нейроэндокринную динамику постпрандиального периода.
Сенсорное насыщение и еда при отсутствии голода
Одним из устойчивых феноменов пищевого поведения является так называемое сенсорно-специфическое насыщение: привлекательность конкретной еды снижается по мере ее потребления, однако другие вкусовые категории могут оставаться высоко желанными. Это создает физиологическую основу для ситуации, когда после плотного основного приема пищи человек сохраняет высокий интерес к десерту.
Таким образом, насыщение не всегда означает завершение пищевого поведения — оно может быть частичным, модально-зависимым и контекстным.
Клинические следствия: ожирение как нарушение регуляции, а не «недостаток воли»
Клиническая картина ожирения, гиперфагии и компульсивного переедания показывает, что устойчивое повышение потребления пищи может формироваться без субъективного ощущения выбора. Системное увеличение калорийности рациона может происходить через небольшие ежедневные изменения — чуть большие порции, более быстрый темп питания, более частые перекусы, усиление тяги — которые накапливаются в течение месяцев и лет.
Дополнительный слой сложности формируется генетическими особенностями: большая часть генетических вариантов, ассоциированных с ожирением, влияет на нейробиологию и регуляторные цепи мозга. Следовательно, у разных людей различаются исходные параметры чувствительности к пищевым сигналам и устойчивость к средовым триггерам.
Клинически это требует перехода от морализаторских интерпретаций к физиологически обоснованной модели: питание является результатом взаимодействия гормональных и нейрональных регуляторов с социальной и пищевой средой.
Заключение: интегративная модель гормональной регуляции питания
Гормональная регуляция питания — это не линейный механизм, а многоуровневая система управления поведением, включающая:
- долгосрочные сигналы энергетических запасов (лептин),
- краткосрочные кишечные сигналы голода и насыщения (грелин, PYY, CCK, GLP-1),
- нейрональные инициаторы голода и поиска пищи (AgRP-нейроны),
- мотивационно-обучающие механизмы системы вознаграждения (дофамин).
Эти элементы функционируют совместно, формируя вероятностную архитектуру пищевого поведения. Для врача, диетолога, эндокринолога и нутрициолога практическая ценность данной модели заключается в том, что она позволяет объяснять пищевые трудности пациента не как «слабость характера», а как результат регулируемой биологии, на которую можно воздействовать через питание, среду, фармакологию и долгосрочную поведенческую поддержку.
- НЕОЖИДАННЫЙ ЭФФЕКТ ПРЕПАРАТОВ ДЛЯ ПОХУДЕНИЯ: КАК ЛЕКАРСТВА ОТ ДИАБЕТА МОГУТ СНИЖАТЬ РИСК ЗАВИСИМОСТЕЙ ОТ НАРКОТИКОВ, АЛКОГОЛЯ И НИКОТИНА
- ЗА ПРЕДЕЛАМИ ТАРЕЛКИ: КАК ПИЩЕВАЯ СРЕДА ОПРЕДЕЛЯЕТ ЗДОРОВЬЕ КАЗАХСТАНА
- МЫ — СОХРАНЕННЫЙ СОЛНЕЧНЫЙ СВЕТ: КАК ЕДА, ЭНЕРГИЯ И СРЕДА ПЕРЕПИСЫВАЮТ СУДЬБУ НАШЕГО ЗДОРОВЬЯ